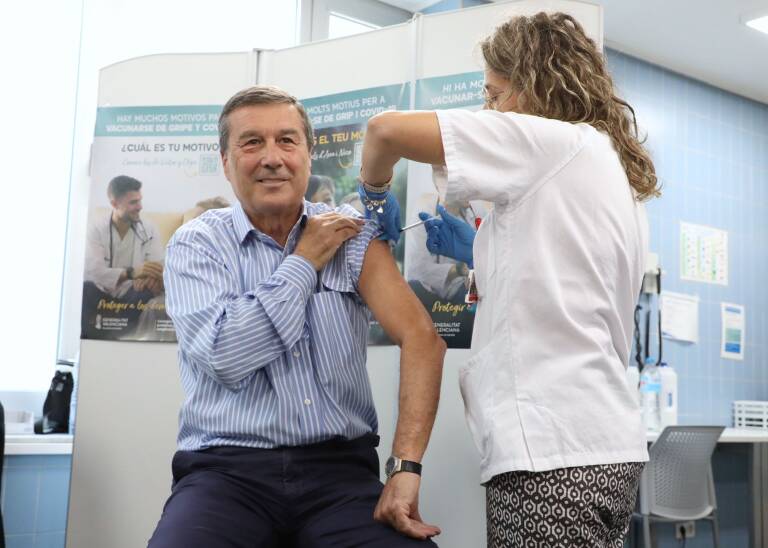
La EMA recomienda la aprobación de la vacuna de Moderna en niños de 6 a 11 años
La EMA avala la dosis de refuerzo de la vacuna de Pfizer a partir de los 12 años
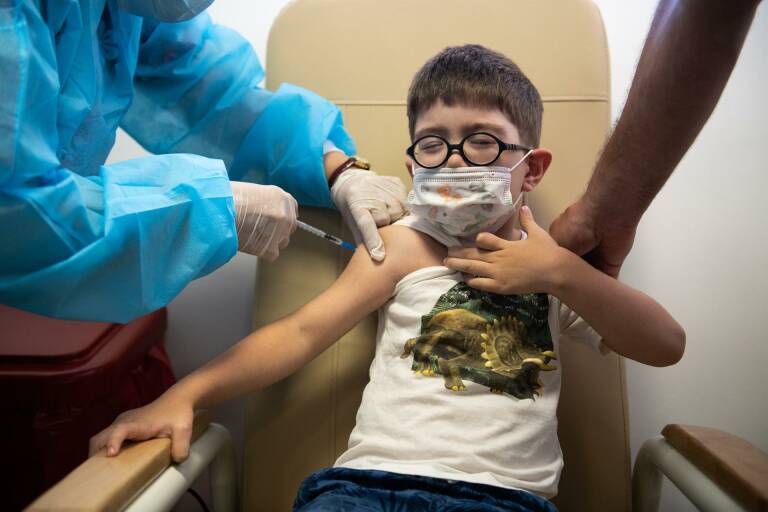
 Foto: EUROPA PRESS
Foto: EUROPA PRESSVALÈNCIA. (EP) El Comité de Medicamentos de Uso Humano (CHMP, por sus siglas en inglés) de la Agencia Europea del Medicamento (EMA, por sus siglas en inglés) ha avalado la dosis de refuerzo de la vacuna contra la COVID-19 de Pfizer a los adolescentes a partir de los 12 años de edad.
Esta vacuna ya está autorizada en la UE como vacunación primaria de 2 dosis en adolescentes (así como en adultos y niños a partir de 5 años) y actualmente está autorizada una dosis de refuerzo a partir de los 18 años. El dictamen del CHMP se remitirá ahora a la Comisión Europea, que emitirá una decisión final "en breve".
El dictamen del CHMP es consecuencia de una evaluación de los datos provisionales de seguridad y eficacia de un ensayo clínico de una dosis de refuerzo de la vacuna en mayores de 16 años, junto con la bibliografía publicada y los datos posteriores a la autorización, además de las pruebas reales del uso de dosis de refuerzo en jóvenes en Israel.
El Comité ha considerado que las pruebas disponibles eran "suficientes para concluir que la respuesta inmunitaria a una dosis de refuerzo en adolescentes sería al menos igual a la de los adultos". Además, no se identificaron nuevos problemas de seguridad a partir de los datos disponibles.
Se esperan más datos de estudios y análisis en adolescentes en los próximos meses. Mientras tanto, la EMA ha indicado que "continuará vigilando y evaluando las pruebas y actualizando la información del producto o tomando otras medidas reglamentarias apropiadas según sea necesario".
En cualquier caso, la decisión sobre si ofrecer dosis de refuerzo en este grupo de edad, y cuándo hacerlo, es decisión de los países europeos y "deberá tener en cuenta factores como la propagación y la probable gravedad de la enfermedad (especialmente con la variante ómicron) en las personas más jóvenes, el riesgo conocido de efectos secundarios (en particular la complicación muy rara pero grave de la miocarditis) y la existencia de otras medidas de protección y restricciones", aclara la EMA.
Moderna
El Comité de Medicamentos de Uso Humano (CHMP, por sus siglas en inglés) de la Agencia Europea del Medicamento (EMA, por sus siglas en inglés) ha recomendado que se amplíe la indicación de la vacuna contra la COVID-19 de Moderna para incluir su uso en niños de 6 a 11 años.
La dosis de la vacuna de Moderna en niños de 6 a 11 años será inferior a la utilizada en personas de 12 años o más (50 ug frente a 100 ug). Al igual que en el grupo de mayor edad, la vacuna se administra en dos inyecciones en los músculos de la parte superior del brazo, con un intervalo de cuatro semanas.
Un estudio principal en niños de 6 a 11 años mostró que la respuesta inmunitaria a la dosis más baja de la vacuna de Moderna (50 ug) era comparable a la observada con la dosis más alta (100 ug) en niños de 18 a 25 años, según el nivel de anticuerpos.
Los efectos secundarios más comunes en los niños de 6 a 11 años son similares a los de los mayores de 12 años. Entre ellos se encuentran dolor, enrojecimiento e hinchazón en el lugar de la inyección, cansancio, dolor de cabeza, escalofríos, náuseas, vómitos, inflamación o sensibilidad de los ganglios linfáticos bajo el brazo, fiebre y dolor muscular y articular. "Estos efectos suelen ser leves o moderados y mejoran a los pocos días de la vacunación", aclara la EMA.
Las pruebas indican que la eficacia y la seguridad de la vacuna de Moderna en niños de 6 a 11 años son "similares" a las de los adultos. Por lo tanto, el CHMP concluyó que los beneficios de la vacuna de Moderna en este grupo de edad "superan los riesgos, especialmente en aquellos con condiciones que aumentan el riesgo de COVID-19 grave".
En cualquier caso, el organismo regulador europeo ha aclarado que la seguridad y la eficacia de la vacuna, tanto en niños como en adultos, "seguirán siendo objeto de un estrecho seguimiento a medida que se utilice en las campañas de vacunación en los Estados miembros de la UE a través del sistema de farmacovigilancia de la UE y de los estudios en curso y adicionales realizados por la empresa y por las autoridades europeas".
El CHMP enviará ahora esta recomendación a la Comisión Europea, que es la encargada de emitir una decisión final. "La recomendación del CHMP de autorizar el uso de nuestra vacuna en niños de 6 a 11 años en Europa es un hito importante. Pone de manifiesto la eficacia y seguridad de nuestra vacuna en este grupo de edad y contribuye a que nuestros niños estén seguros y puedan llevar una vida escolar y familiar normal. Estamos agradecidos al CHMP por su exhaustiva revisión de nuestra presentación y esperamos una decisión de autorización por parte de la Comisión Europea", ha comentado el director general de Moderna, Stéphane Bancel.
Por otra parte, según ha anunciado Moderna, la EMA también ha recomendado actualizaciones en el uso de la vacuna. Ahora, la dosis de refuerzo de 50 ug, indicada para personas de 18 años o más, se recomienda al menos tres meses después de la segunda dosis. Este plazo se ha acortado respecto al anteriormente aprobado de seis meses.
Los cambios también incluyen la posibilidad de administrar una dosis de refuerzo heteróloga (mixta), tras completar la vacunación primaria con otra vacuna autorizada contra la COVID-19.